CHẤT
LƯỢNG NƯỚC - XÁC ĐỊNH XYANUA - PHẦN 3: XÁC ĐỊNH XYANOGEN CLORUA
Water quality - Determination of
cyanide - Part 3: Determination of cyanogen chloride
Lời nói đầu
TCVN 6181-3:2015 hoàn toàn tương đương với
ISO 6703-3:1984 đã được rà soát và phê duyệt lại vào năm 2012 với bố cục và nội
dung không thay đổi.
TCVN 6181-3:2015 do Ban kỹ thuật tiêu chuẩn
quốc gia TCVN/TC 147 Chất lượng nước
biên soạn, Tổng cục Tiêu chuẩn Đo lường Chất lượng đề nghị, Bộ Khoa học và Công
nghệ công bố.
Bộ
tiêu chuẩn TCVN 6181 (ISO 6703), Chất lượng nước - Xác định xyanua gồm
các tiêu
chuẩn sau:
- TCVN
6181-1:1996 (ISO 6703-1:1984),
Phần 1: Xác định xyanua tổng;
- TCVN
6181-2:2015 (ISO 6703-2:1984), Phần
2: Xác định xyanua dễ giải phóng;
- TCVN
6181-3:2015 (ISO 6703-3:1984), Phần 3: Xác định xyanogen clorua.
CHẤT LƯỢNG NƯỚC - XÁC ĐỊNH
XYANUA - PHẦN 3: XÁC ĐỊNH XYANOGEN
CLORUA
Water quality
- Determination of cyanide - Part 3: Determination of cyanogen chloride
CẢNH BÁO: Cần chú ý tới độc tính của
xyanua và
phải đặc biệt cẩn trọng khi xử lý xyanua và các dung dịch của chúng.
Tất cả mọi thao tác phải thực hiện
trong tủ hút. Tránh tiếp xúc với da và mắt. Khi hút luôn luôn sử dụng pipet
an toàn
(pipet có quả bóp). Việc khử độc các mẫu và các dung dịch có chứa xyanua
hay các kim loại nặng tuân theo các quy định của cơ quan quản lý có thẩm quyền.
Các hóa chất khác được quy định trong
tiêu
chuẩn này đều
nguy hại,
ví
dụ như pyridin.
Tiêu
chuẩn này quy định phương pháp xác định các xyanua theo xyanogen clorua trong nước (xem Điều
2).
Phương
pháp có thể
áp dụng để xác định
nồng độ xyanogen clorua trong khoảng từ 0,02 mg/L đến 15 mg/L.
Nhiều
ion và các hợp chất được liệt kê trong Bảng 1, nếu chúng tồn tại độc lập hay kết
hợp ở nồng độ của chúng ở trên nồng
độ giới hạn đã quy định thì gây cản trở
đến phương pháp (danh sách
này chưa nêu đầy đủ các chất gây cản trở).
Sự
có mặt của các
andehyt, ví dụ formandehyt làm chỉ số
xyanua thấp do hình
thành xianohydrin.
Bảng 1 - Chất
cản trở
|
Chất cản trở |
Nồng độ giới
hạn mg/L |
|
lon
suntit |
1000 |
|
lon
polysunfit |
300 |
|
lon
sunfit và polysunfit |
1000 |
|
Ion
sunfit |
500 |
|
lon
sunfat |
1000 |
|
lon
thioxyanat |
1000 |
|
Clorua
(nguyên tố) |
250 |
Tiêu chuẩn này áp dụng các thuật
ngữ định nghĩa sau:
2.1
Xyanogen clorua (cyanogen chloride)
Sản phẩm phản ứng đầu tiên khi các hợp
chất xyanua bị clo hóa.
Xyanogen
clorua là một khí
và chỉ hòa tan ít trong nước, nhưng có độc tính cao ngay cả ở nồng độ thấp.
Dung
dịch thiếc (II) clorua
được bổ sung
vào mẫu và lôi cuốn xyanogen clorua đã
giải phóng ở pH = 5,4 và nhiệt độ phòng bằng lôi
cuốn theo một dòng khí vào
dung dịch hấp thụ có chứa pyridin/axit bacbituric. Xác định nồng độ xyanogen
clorua bằng đo quang.
Tất cả các thuốc thử đạt cấp phân tích được công nhận và nước được
sử dụng là nước cất
hoặc nước đã loại ion.
4.1 Axit
clohydric, dung
dịch, ρ = 1,12 g/mL.
4.2 Axit clohydric, dung dịch, c(HCI) = 1 mol/L.
4.3 Thiếc (II)
clorua,
dung dịch.
Hòa
tan 50 g thiếc (II) clorua ngậm hai phân tử
nước (SnCl2.2H2O)
trong dung dịch axit clohydric (4.2) và cũng pha loãng bằng dung dịch axit clohydric
tới 100 mL.
Chuẩn
bị dung dịch mới hàng tuần.
4.4 Natri clorua,
dung dịch,
c(NaCI) = 0,5 mol/L.
4.5 Natri
hydroxit,
dung dịch, c(NaOH) = 0,4 mol/L.
4.6 Pyridin/axit
bacbituric,
dung dịch.
Cho
3 g axit bacbituric (C4N4N2O3) vào bình định mức một vạch
dung tích 50 mL, tráng thành bình
bằng lượng nước vừa đủ để làm
ẩm axit bacbituric, thêm 15 mL pyridin (C5H5N) và khuấy cho tới khi trộn đều.
Thêm 3 mL dung dịch axit clohydric
(4.1) và pha loãng tới vạch bằng nước.
Bảo
quản qua đêm trong tủ lạnh và nếu
cần, lọc
để loại
bỏ mọi
axit bacbituric không tan.
Dung
dịch ổn định khoảng một ngày nếu
được bảo quản trong tối và khoảng một tuần nếu được bảo quản trong tủ tạnh.
4.7 Kali xyanua, dung dịch tiêu chuẩn tương
ứng với 10 mg CN-/L.
Hòa
tan 25 mg kali xyanua trong dung dịch natri hydroxit (4.5) và pha loãng tới 1000 mL
trong bình định
mức một vạch bằng chính dung dịch natri hydroxit này.
Chuẩn hóa dung dịch này bằng chuẩn độ với
dung dịch bạc nitrat (4.8) ngay trước khi sử dụng hoặc hàng ngày, nếu tiến hành một
số lượng lớn các phép thử.
4.8 Bạc nitrat, dung dịch c(AgNO3) = 0,01 mol/L.
Bảo
quản trong chai tối màu.
4.9 Dung dịch đệm, có pH = 5,4.
Hòa
tan 6 g natri hydroxit
trong khoảng 50 mL nước, thêm 11,8 g axit sucxinic (C4H6O4) và pha loãng bằng nước tới
100 mL.
4.10 Cloramin-T, dung dịch.
Hòa
tan 0,5 g Cloramin-T
ngậm ba phân tử nước (C7H7CINaNSO2.3H2O) với nước trong bình định
mức một vạch 50 mL và pha loãng tới vạch bằng nước.
Chuẩn
bị dung dịch mới hàng
tuần. Kiểm tra từng mẻ
cloramin-T dựa theo đường hiệu chuẩn.
Thiết
bị, dụng cụ
của phòng thử
nghiệm thông thường, và
5.1 Bình chưng cất 3 cổ, dung tích 500 mL, có các chỗ
nối hình nón chuẩn
(cổ giữa 29/32, các cổ bên cạnh 14,5/23 như đã nêu trong Hình 1).
5.2 Bình hấp thụ, bảo vệ chất lỏng chảy ngược, bằng thủy tinh xốp
G1 (xem Hình 2).
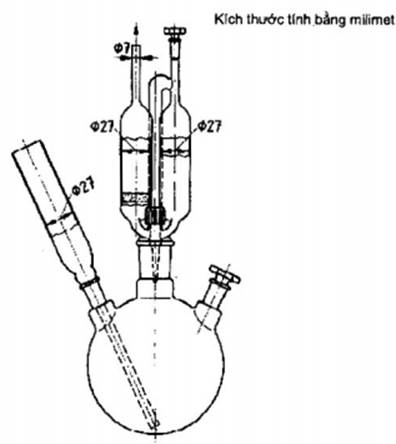
Hình 1 - Bình chưng cất ba cổ
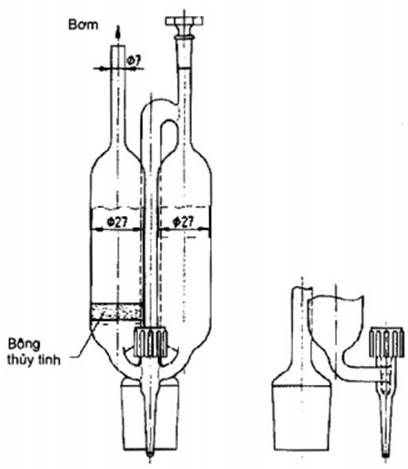
Hình 2 - Bình
hấp thụ
|
Hình 3 - Phễu tách |
Hình 4 - Phễu
lấy
mẫu 10 mL |
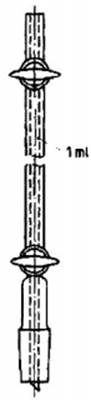
Hình 5 - Phễu
lấy mẫu 1 mL
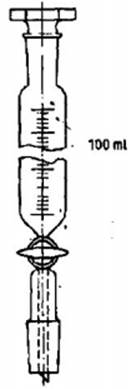
5.3 Phễu tách1 dung tích 100 mL (xem Hình
3).
5.4 Phễu lấy mẫu1 dung tích 10 mL
(xem Hình 4).
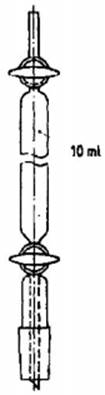
5.5 Phễu lấy mẫu1 dung tích 1 mL (xem Hình 5).
5.6 Bình định mức,
dung tích 25 mL, 50 mL, 250 mL và
1 000 mL.
5.7 Lưu lượng kế
5.8 Máy đo quang,
với cuvet
có chiều dài quang 10 mm.
Đối với
các nồng độ xyanogen clorua dự tính nhỏ hơn 0,15 mg/L, lấy mẫu bằng phễu tách (5.3).
Đối với các nồng độ dự tính giữa khoảng từ 0,15 mg/L đến 1,5 mg/L, lấy mẫu trong phễu
láy mẫu 10 mL (5.4) và đối với các nồng độ dự tính ở giữa khoảng từ 1,5 mg/L đến 15
mg/L, lấy mẫu bằng
phễu lấy mẫu 1 mL. (5.5).
Tiến hành lấy mẫu bằng cách
nhúng ngập phễu thích hợp vào nước để
lấy mẫu (đóng van ngắt bên dưới bề mặt nước). Nếu sử dụng phễu tách (5.3), cho 5 mL dung dịch
thiếc (II) clorua (4.3) vào phễu trước khi lấy mẫu. Nút ngay phễu.
Nếu
sử dụng một phễu lấy
mẫu (5.4 hoặc 5.5) để lấy mẫu, cho 5 mL dung dịch thiếc (II) clorua (4.3) vào phễu tách
(5.3) và pha loãng bằng
nước tới 100 mL.
Tráng
phễu lấy mẫu (5.4 hoặc 5.5) bằng nước và
cho nước đó vào trong phễu
tách (5.3). Mở van ngắt của phễu tách
thứ nhất, sau
đó mở van ngắt của phễu lấy mẫu thấp hơn,
cuối cùng mở van ngắt của phễu cao hơn. Sau khi nước chảy ra khỏi van ngắt lấy
mẫu khoảng
20 mL, đóng van
ngắt của phễu tách, bỏ phễu lấy mẫu và nút ngay phễu tách.
Phân
tích mẫu càng sớm càng
tốt. Nếu cần bảo quản thì giữ mẫu trong tối và chỗ mát.
7.1 Tách xyanogen
clorua
Cho
bình hấp
thụ (5.2) vào cổ giữa của bình chưng cất
ba cổ (5.1) và rót 2 mL dung dịch đệm (4.9), 3 mL dung dịch pyridin/axit
bacbituric (4.6), 8 mL dung dịch natri clorua (4.4) và khoảng 8 mL nước vào bình hấp thụ. (Dung dịch hấp thụ này có thể được trộn
đều, trước khi sử dụng, trong bình tối
màu; dung dịch hỗn
hợp này ổn định
khoảng vài ngày ở nhiệt độ phòng).
Nối bình
hấp
thụ với bơm và điều chỉnh
dòng khí tới khoảng 40 L/h.
Cho phễu tách (5.3) vào một cổ bên và một phễu khác (5.4 hoặc 5.5) với cổ bên
thứ hai. Rót 10 mL dung dịch đệm (4.9) vào bình nón. Mở van ngắt của phễu tách và
di chuyển nút cẩn
thận để cho
khí đi vào. Khi phễu tách rỗng, bỏ nút và tráng phễu bằng một lượng nước nhỏ.
Sau
1 min, đóng
van ngắt của phễu tách, sao cho dòng
khí đi vào bình nón qua phễu còn
lại.
Sau
20 min, tháo bộ phận nối cung cấp khí. Chuyển các thành phần chứa của bình hấp
thụ vào bình định mức, tráng bình bằng một phần nước rất nhỏ, pha loãng tới vạch và trộn
đều.
7.2 Phép thử trắng
Tiến
hành phép thử trắng song song với phép xác định, sử dụng cùng loại thuốc thử với
cùng lượng và theo cùng một quy trình,
nhưng thay mẫu thử bằng nước.
7.3 Xác định
Ngay
sau khi tách xyanogen clorua (không quá 10 min), đo độ hấp thụ của dung dịch hấp thụ
ở 578 nm, sử dụng dung dịch thử trắng (7.2), làm dịch lỏng chuẩn.
7.4 Chuẩn bị đồ thị hiệu chuẩn
7.4.1 Chuẩn
bị dung chuẩn phù
hợp
Sử dụng
pipet
chuyển 2 mL, 5 mL,
20 mL và 25 mL, lần lượt, dung dịch kali xyanua tiêu chuẩn (4.7) vào trong một dãy
bốn bình
định mức một vạch dung tích 250 ml (5.6). Pha loãng tới vạch bằng dung dịch natri
hydroxit (4.5) và trộn đều.
Sử dụng
pipet chuyển 10 mL từng dung dịch này vào bình định mức một vạch dung tích 25 mL (5.6) và vừa thêm
vừa trộn 2 mL dung dịch đệm (4.9), 4 mL dung dịch axít clohydric (4.2) và 1 mL
dung dịch clororamin-T
(4.10). Đóng nút bình và để yên 5 min ± 1 min.
Thêm
3 mL dung dịch pyridin/axit bactiburic (4.6) pha loãng tới vạch bằng nước và trộn
đều.
7.4.2 Phép
đo quang
Đo độ
hấp thụ
của từng dung dịch ở 578 nm trong ngăn đo có chiều dài quang 10 mm dựa theo
dung dịch chuẩn2. Tiến hành các phép đo 20
min ± 5 min sau khi thêm dung dịch pyridin/axit bacbituric.
7.4.3 Dựng đồ thị
Dựng
đồ thị của độ hấp thụ dựa theo các hàm tượng xyanua của dung dịch, tính bằng
miligam. Tương quan giữa độ hấp
thụ và nồng độ là tuyến tính. Thường xuyên kiểm đồ thị, đặc biệt, nếu sử dụng các gói hóa chất mới.
Kiểm
tra các giá trị tuyệt đối của đồ thị hiệu chuẩn bằng chuẩn độ dung dịch tiêu chuẩn
hiệu chuẩn bằng dung dịch bạc nitrat.
Nồng
độ xyanogen clorua, tính
bằng miligam trên
lít, được tính theo Công thức:
![]()
Trong
đó:
m là hàm lượng xyanua đọc từ đường hiệu chuẩn, tính bằng
miligam;
V là thể tích của mẫu, tính bằng mililit;
2,36
là hệ số chuyển đổi để biểu thị xyanua theo xyanogen clorua.
Báo
cáo các kết quả tính bằng miligam trên lít.
Phương
pháp này là không thích hợp đối với phép
thử liên phòng thử nghiệm vì không
thể chuẩn bị và phân bổ
các dung dịch xyanogen clorua ổn định.
Báo
cáo thử phải bao gồm các thông
tin sau:
a) Viện
dẫn tiêu chuẩn này;
b) Các
kết quả và đơn vị được sử dụng;
c) Mọi
dấu hiệu bất thường được ghi nhận trong quá
trình xác định;
d) Các
chi tiết của mọi quy trình
không quy định trong tiêu chuẩn này,
hoặc các chi tiết bất
thường khác làm
ảnh hưởng đến kết quả.
THƯ MỤC TÀI
LIỆU THAM KHẢO
[1]
Mertens, H., Z.f. Wasser und Abwasser- Forschung, 9 (1976), pp. 183 - 195.
[2]
Mertens, H., Vom Wasser, 52 (1979), pp. 61 - 74.